医疗器械软件标准与检测下的软件设计与开发关键点
医疗器械软件的开发需严格遵循相关标准,以确保软件的安全性和有效性,并通过检测环节验证其合规性。本文将从软件设计与开发阶段出发,结合关键标准要求,探讨医疗器械软件的高质量实现路径。
一、医疗器械软件标准体系概述
医疗器械软件设计开发需遵循的国家及国际标准包括:YY/T 0664-2021《医疗器械软件 软件生存周期过程》、IEC 62304《医疗器械软件 软件生存周期过程》等。这些标准明确了软件生存周期的各个阶段要求,从需求分析到设计、实现、验证、确认及维护,强调了风险管理、可追溯性与文档化的重要性。在设计与开发中,必须将这些标准融入流程,确保软件的可靠性和合规性。
二、软件设计阶段的关键原则
- 需求分析:软件设计始于准确的需求分析,需明确功能需求、性能需求和安全性需求。标准要求需求必须可验证,并与风险管理相结合,识别潜在危害。
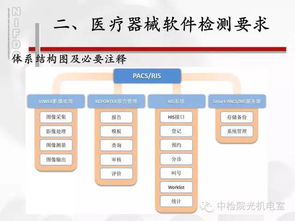
- 架构设计:采用模块化设计,提高软件的可维护性和可测试性。架构应支持数据的完整性、保密性和可用性,例如通过冗余机制或错误处理模块。
- 用户界面设计:界面需直观易用,符合人因工程学原则,减少用户操作错误,这对于高风险医疗器械尤为重要。
三、软件开发中的实施要点
- 编码规范:使用一致的编码标准和工具,确保代码的可读性和可维护性。实施版本控制(如Git)和代码审查,以早期发现缺陷。
- 单元测试与集成测试:在开发过程中进行充分的测试,包括单元测试验证单个模块功能,以及集成测试检查模块间交互。这需与风险管理结合,针对高风险功能进行重点测试。
- 文档记录:详细记录设计决策、代码注释和测试用例,便于后续验证和监管审查。标准要求文档可追溯至需求,确保全生命周期可管理。
四、检测与验证环节
软件开发完成后,需通过独立的检测流程,包括:
- 验证测试:确认软件满足指定需求,通常通过黑盒和白盒测试方法。
- 确认测试:在模拟或真实环境中验证软件的性能和安全性,确保其适用于预期用途。
- 合规性检查:依据标准如IEC 62304,审核软件生存周期文档和风险管理报告,确保符合法规要求。
检测中发现的问题需反馈至开发阶段进行迭代改进,形成闭环管理。
五、总结与建议
医疗器械软件的设计与开发是一个系统化过程,必须将标准要求融入每个环节。开发团队应建立质量管理体系,强化风险管理和测试验证,同时关注新兴技术如人工智能在医疗软件中的应用挑战。通过严格遵循标准与检测流程,可以交付安全、有效的医疗器械软件,保障患者安全和医疗质量。
如若转载,请注明出处:http://www.zhenxunkeji.com/product/21.html
更新时间:2025-11-28 18:29:13